Этановая кислота. 20 применений уксуса в хозяйстве, о которых вы не знали!
- Этановая кислота. 20 применений уксуса в хозяйстве, о которых вы не знали!
- Этановая кислота формула. Этановая кислота. Физические свойства, получение и применение
- Этановая кислота интересные факты. Интересные факты про кислоты
- Пропановая кислота. Формула пропановой кислоты
- Определение и формула пропановой кислоты
- Химическая формула пропановой кислоты
- Структурная (графическая) формула пропановой кислоты
- Примеры решения задач
- Видео Ледяная уксусная кислота
- Уксусная кислота 3%. Что такое уксусная кислота
- Этановая кислота. Что такое уксусная кислота
- Чем опасна уксусная кислота. Когда вреден столовый уксус
Этановая кислота. 20 применений уксуса в хозяйстве, о которых вы не знали!
Уксус, без сомнения, найдется на каждой кухне. А вот область его применения намного шире, чем кулинария. Уксус поможет вам:
1 избавиться от сорняков. Пролейте их, разведя уксус (40%) водой пополам.
2 удалить пятна пота с одежды. Перед стиркой на 10 мин. Смочите пятно пота белым столовым уксусом, и оно сойдет очень легко.
3 вылечить ангину. Разведите в стакане теплой воды 1 ст. л. яблочного уксуса и прополощите горло.
 4 сделать волосы послушными. После мытья ополаскивайте волосы раствором яблочного уксуса (1/2 ст. л. на стакан воды.
4 сделать волосы послушными. После мытья ополаскивайте волосы раствором яблочного уксуса (1/2 ст. л. на стакан воды.
5 снять мышечную боль. После интенсивных нагрузок в мышцах накапливается молочная кислота, которая вызывает боль. Снять ее, растворив кислоту, поможет 20-минутный уксусный компресс (2-3 ст. л. на стакан воды.
6 отклеить ценник. Слегка подогрейте белый уксус, смочите в нем губку и приложите к наклейке. Она отклеится, не оставив липких следов.
7 снять ржавчину. Мелкие заржавленные предметы (болты, гайки, гвозди и т. п. ) прокипятите с уксусом, а потом хорошо промойте водой.
8 убрать затхлый запах. Протрите поверхности холодильника, шкафа или пищевого контейнера тряпкой, смоченной в уксусе.
9 удалить накипь. Прокипятите воду с добавлением уксуса в чайнике или добавьте его в отсек для ополаскивателя при стирке. Уксус отлично снимает известковые отложения.
10 исправить вкус испорченного блюда. Таким образом, если вы переперчили суп, для нейтрализации пряности добавьте в кастрюлю 1 ч. л. яблочного уксуса.
11 сохранить цвет одежды. Для этого добавьте 0, 5 стакана уксуса в барабан стиральной машины при стирке.
12 освежить воздух. Магазинные освежители воздуха часто обладают резким запахом, который смешивается с остальными и образует еще более неприятный. Протрите раствором столового уксуса поверхности в комнате, разбрызгайте его по углам, и сами не заметите, как неприятный запах исчезнет.
13 растворить засохшую краску на кисти. Вскипятите немного уксуса в кастрюле, опустите в нее кисточку и слегка потрите о дно. Краска сойдет.
14 избавиться от муравьев. Раз - ведите уксус водой пополам и распылите в месте, где появились насекомые. Уксус сотрет следы муравьев, и за ними не потянутся их сородичи.
15 унять икоту. Смочите в уксусе кусочек сахара, быстро раскусите и проглотите.
16 помыть стекла, пластик и хром. Разведите уксус водой пополам и протрите загрязненные поверхности. Смешайте немного уксуса с содой, чтобы отчистить до блеска нержавейку и хром.
17 продлить жизнь букета. Добавив 2 ст. л. на 1 л воды в вазу, где стоят срезанные цветы, вы сможете любоваться ими намного дольше.
18 вылечить грибок на ногах. Раз в несколько дней в течение 15-20 мин. Принимайте ванночку из уксуса с водой (1: 5.
19 приготовить вкусное мясо для шашлыка. Стакан столового уксуса на 2 стакана воды плюс специи - отличный маринад, гарантирующий сочное мягкое мясо.
20 устранить засор. Помощь сантехника может и не понадобиться, если высыпать в засорившийся сток 3/4 стакана соды и залить ее 1/2 стакана уксуса. Через 30 мин. Пролейте сток чайником кипятка. Таким образом удаляются даже стойкие засоры.
Этановая кислота формула. Этановая кислота. Физические свойства, получение и применение
Этановая кислота (другое название - уксусная) - это органическое вещество, представляющее собой предельно основную, слабую, карбоновую кислоту. Производные данной кислоты называются ацетатами. При помощи этого вещества можно получить метиловый эфир этановой кислоты: этаналь + этановая кислота = метиловый эфир.
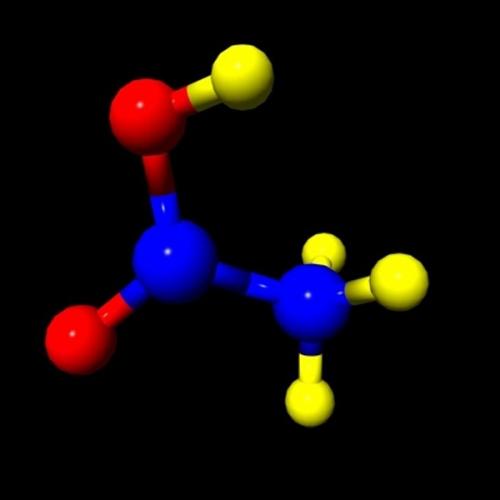
Физические свойства этановой кислоты
1. Этановая кислота (формула - CH3COOH) представляет собой жидкость без цвета со специфическим запахом и неприятным кислым вкусом.
2. Гигроскопична. В воде неограниченно растворима.
3. Этановая кислота смешивается с большинством растворителей. В ней хорошо растворяются неорганические газы и соединения, такие как HI (йодоводород), HF (фтороводород), HBr (бромоводород), HCl (кислота соляная) и многие другие.
4. Существует в виде линейных и циклических димеров.
5. Диэлектрическая проницаемость составляет 6,1.
6. Температура самовоспламенения на воздухе равна 454 градусам.
7. Этановая кислота образует азеотропные смеси с четыреххлористым углеродом, бензолом, циклогексаном, толуолом, гептаном, этилбензолом, трихлорэтиленом, о-ксилолом, п-ксилолом и бромофором.
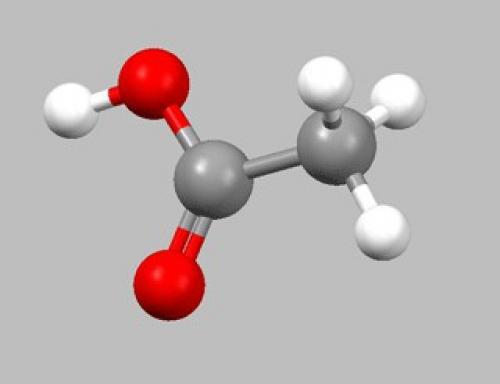
Этановую кислоту можно получить несколькими способами:
1. Путем окисления ацетальдегида кислородом из воздуха. Данный процесс возможен только в присутствии катализатора - марганца ацетата при температуре от 50 до 60 градусов. Реакция выглядит так:
2CH3CHO (ацетальдегид) + O2 (кислород) = 2CH3COOH (этановая кислота)
2. В промышленности используют окислительные способы. Раньше для получения этановой кислоты применяли окисление бутана и ацетальдегида.
Ацетилальдегид окисляли только в присутствии марганца ацетата при повышенном давлении и температуре. При этом выход этановой кислоты составлял около девяноста пяти процентов.
2CH3CHO + O2 = 2CH3COOH
Н-бутан окисляли при температуре от 150 до 200 градусов. При этом ацетат кобальта выполнял роль катализатора.
2C4H10 + 5O2 = 4CH3COOH + 2H2O
Но в результате значительного повышения цен на нефть оба эти способа стали невыгодными и вскоре оказались вытеснены более эффективными способами карбонилирования метанола.
3. Карбонилирование метанола каталитическое - это важный способ синтеза этановой кислоты. Происходит по условному уравнению:
CH3OH + CO = CH3COOH
4. Также существует биохимический способ получения, при котором используется способность микроорганизмов окислять этанол. Данный процесс называется уксуснокислым брожением. При этом в качестве сырья используют водный эфир спирта этилового или этанолосодержащие жидкости (забродившие соки). Это многоступенчатый сложный процесс. Его можно описать следующим уравнением:
CH3CH2OH (эфир спирта) + O2 (кислород) = CH3COOH (этановая кислота) + H2O

Применение
- водные растворы этановой кислоты применяются в пищевой промышленности, кулинарии и в консервировании;
- этановая кислота используется для создания душистых веществ и лекарственных препаратов (ацетон, ацетилцеллюлоза);
- применяется в крашении и книгопечатании;
- в качестве реакционной среды для окислении некоторых органических веществ (окисление сульфидов пероксидом водорода);
- так как пары этановой кислоты обладают неприятным резким запахом, то его можно использовать вместо нашатырного спирта.
Этановая кислота интересные факты. Интересные факты про кислоты

Самой первой кислотой, которую удалось выделить и использовать человечеству, конечно, была уксусная. Да и сам термин «кислота» (от латинского «acid») вероятно произошел от латинского «acetum» - уксус. Нарушение технологии, при производстве вина виноделами древности, приводило к его скисанию и образованию уксуса. На первых порах его выливали, но затем нашли применение в качестве приправы, лекарства и растворителя.

В 1778 году французский химик Антуан Лавуазье предположил, что кислотные свойства обусловлены наличием в их составе кислорода. Эта гипотеза оказалась несостоятельной, так как многие кислоты не имеют в своём составе кислорода, в то время как многие кислородсодержащие соединения не проявляют кислотных свойств. Тем не менее, именно эта гипотеза дала название кислороду как химическому элементу. И только в 1833 году немецкий химик Юстус Либих определил кислоту, как водородсодержащее соединение, в котором водород может быть замещён на металл.
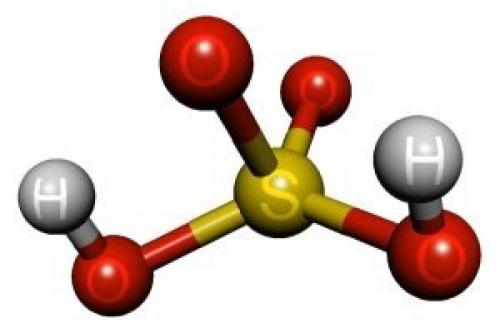
Степень кислотности раствора определяется концентрацией в нем водородных ионов, которую обычно выражают количеством грамм-ионов на I л. Для удобства кислотность растворов принято выражат в так называемой величиной рН. Дисцилированная вода имеет pH=7, если ниже то раствор становится кислотным, а выше - щелочным. Измерения проводят по шкале от 0 до 14.

Желудок человека вынужден ежедневно обновлять свою поверхность взамен пострадавшей от желудочного сока, то есть соляной кислоты. Желудочный сок человека достаточно агрессивен для того, чтобы полностью растворить бритвенное лезвие за неделю.
Смесь двух кислот азотной и соляной в пропорции 1 к 3, представляет собой жидкость желтого цвета и обладает уникальной способностью растворять многие благородные металлы (золото, платину), за что получила название «Царской водки».

Не многие знают, что важным ингредиентом популярной Кока-колы является ортофосфорная кислота, с показателем кислотности рН=2.8.
Муравьиная кислота названа так потому, что в момент опасности выделяется муравьями для предупреждения других обитателей муравейника, и защиты от хищников.
У теплокровных животных в процессе обмена веществ вырабатывается небольшое количество молочной кислоты, и ее запах позволяет комарам и другим кровососущим насекомым находить свои жертвы.

Витамин С или аскорбиновая кислота имеет формулу C6H8O6 и является водорастворимым витамином участвующим в биохимических окислительно-восстановительных процессах человеческого организма.
Лимонную кислоту получают не только из лимонов (25кг на тонну лимонов), но и из плесневого гриба Aspergillus niger.
Пропановая кислота. Формула пропановой кислоты
Определение и формула пропановой кислоты
ОПРЕДЕЛЕНИЕ
Пропановая (припионовая, метилуксусная) кислота – это сложное органическое соединение, относящееся к классу предельных одноосновных карбоновых кислот.
В обычных условиях представляет собой бесцветную едкую жидкость с резким запахом. Самовоспламеняется при температуре 440oC. Смешивается с водой и органическими растворителями.
Химическая формула пропановой кислоты
Химическая формула пропановой кислоты может записываться двояко: C2H5COOH или C3H6O2. Она показывает, что в состав данной молекулы входят три атома углерода (Ar = 12 а.е.м.), шесть атомов водорода (Ar= 1 а.е.м.) и два атома кислорода (Ar = 16 а.е.м.). По химической формуле можно вычислить молекулярную массу пропановой кислоты:
Структурная (графическая) формула пропановой кислоты
Структурная (графическая) формула пропановой кислоты является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы (рис. 1).
Рис. 1. Пропановая кислота. Графическая формула.
Примеры решения задач
ПРИМЕР 1
| Задание | При нейтрализации 25,5 г предельной одноосновной кислоты избытком раствора гидрокарбоната натрия выделилось 5,6 л (н.у.) газа. Определите молекулярную формулу кислоты. |
| Решение | Запишем уравнение реакции нейтрализации предельной одноосновной кислоты избытком раствора гидрокарбоната натрия в общем виде: CnH2n+1COOH + NaHCO3→ CnH2n+1COONa + CO2↑ + H2O. Рассчитаем количество вещества выделившегося в ходе реакции углекислого газа: n = V / Vm; n(CO2) = V(CO2) / Vm; n(CO2) = 5,6 / 22,4 = 0,25 моль. Согласно уравнению реакции n(CO2): n(CnH2n+1COOH) = 1:1, т.е. n(CnH2n+1COOH) = n(CO2) = 0,25 моль. Рассчитаем молярную массу предельной одноосновной кислоты: M = m / n; M(CnH2n+1COOH) = m(CnH2n+1COOH) / n(CnH2n+1COOH); M(CnH2n+1COOH) = 25,5 / 0,25 = 102 г/моль. Определим число атомов углерода в молекуле предельной одноосновной кислоты (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел: 12 – для углерода, 1 – для водорода и 16 для кислорода): M(CnH2n+1COOH) = 12n + 2n + 1 + 12 + 16 + 16 +1 = 14n + 46; 14n + 46 = 102 г/моль; 14n = 56; n = 4. Значит молекулярная формула предельной одноосновной кислоты C4H9COOH. |
Видео Ледяная уксусная кислота
Уксусная кислота 3%. Что такое уксусная кислота
Уксусная кислота – это органический продукт со специфическим запахом и вкусом, представляет собой результат брожения спиртовых и углеводных компонентов либо скисания вин.
Это вещество в форме винного уксуса было известно еще в Древней Греции и Древнем Риме. В более поздние времена алхимики научились производить более чистую субстанцию в результате перегонки. Кислота в виде кристаллов была выведена в 1700 году. Приблизительно в это же время химики определили ее формулу и заприметили способность вещества к воспламенению.
В природе уксусная кислота редко встречается в свободном виде. В составе растений она представлена в форме солей или эфиров, в теле животных найдена в составе мышечной ткани, селезенки, а также в моче, поте, экскрементах. Легко образуется вследствие брожения, гниения, в процессе распада сложных органических соединений.
Синтетическую форму уксусной кислоты получают после реакции воздействия углекислотой на натрий-метил либо же при воздействии на метилат натрия, нагретый до 160 градусов, окисью углерода. Есть и другие способы создания этой субстанции в лаборатории.
Чистая уксусная кислота – это прозрачная жидкость с удушливым запахом, вызывающая ожоги на теле. Если зажечь пары вещества, они дадут светло-голубое пламя. Растворяясь в воде, кислота выделяет тепло.
Ацетилкофермент А образовывается при участии уксусной кислоты, которая также необходима для биосинтеза стеринов, жирных кислот, стероидов и других веществ. Химические свойства уксусной кислоты делают ее незаменимой во многих процессах и реакциях. Уксусная кислота помогает образовывать соли, амиды, сложные эфиры.
Но помимо полезных свойств, является опасным, легковоспламеняющимся веществом. Поэтому работая с ним, необходимо максимально соблюдать технику безопасности, избегая прямого контакта с кожей, стараясь не дышать кислотными парами.
Формы уксусной кислоты:
- ледяная (96-процентный раствор, применяют для удаления бородавок, мозолей);
- эссенция (содержит 30-80 процентов кислоты, входит в состав медпрепаратов против грибков и зуда);
- уксус столовый (3-, 6-, 9-процентный раствор, активно применяется в быту);
- яблочный (или другой фруктово-ягодный) уксус (с низким процентом кислотности, применяется в кулинарии, косметологии);
- уксус бальзамический, или ароматный (столовый уксус, настоянный на пряных растениях, применяется в кулинарии и косметологии);
- ацетат (эфир кислоты).
Этановая кислота. Что такое уксусная кислота
Это синтетический продукт, образованный путем брожения этанола и углеводов или после естественного скисания сухих винных сортов. Этановая кислота принимает участие в обменных процессах, осуществляющихся в организме человека. Кислую жидкость, кроме того, используют для приготовления консервации, маринадов. Определенные свойства продукта делают его незаменимым во множестве химических соединений, средствах бытового значения.
Формула
В состав уксусной кислоты входит уксус 3-9% уксус и 70-80% уксусная эссенция. Соли и эфиры продукта называются ацетатами. Обычный уксус, который используется в кулинарии, содержит яблочную, аскорбиновую, уксусную и молочную кислоты. Ежегодно в мире производят около 5 миллионов тонн этановая кислоты. Ее химическая формула имеет следующий вид: C2H4O2.
Получение
Из чего делают уксусную кислоту сегодня? Для получения жидкости технического назначения используется древесный черный порошок, который содержит большое количество смолистых веществ. Самым выгодным химическим способом получения продукта является окисления этаналя или ацетальдегида, который в промышленности получают либо посредством гидратации ацетилена с солями ртути (метод называют реакцией Чугаева) или же окислением этилового спирта над раскаленной медью. Ацетальдегид самостоятельно окисляется кислородом и трансформируется в уксусную кислоту.
Раствор уксусной кислоты транспортируется на разные расстояния в автомобильных или железнодорожных цистернах, произведенных из специальных видов нержавеющих стальных материалов. На складах жидкость хранится в герметичных контейнерах, емкостях, бочках под навесами либо в специальных помещениях. Заливать и хранить кислоту в полимерной таре допускается максимум на протяжении одного месяца.

Концентрация
Растворы уксусной кислоты, которые применяются пищевой промышленностью, бытовой кулинарии, консервации, называются уксусом и уксусной эссенцией. Абсолютная концентрированная кислота называется ледяной, поскольку при замерзании она преобразуется в массу, напоминающую по структуре лед. Разная концентрация уксусной кислоты обуславливает следующую классификацию продукта:
- эссенция (содержит 30-80% кислоты, является компонентом медикаментов от зуда, грибков);
- ледяная (раствор 96%, используется для удаления мозолей, бородавок);
- столовый уксус (имеет концентрацию 3, 6 или 9%, активно используется для бытовых целей);
- ацетатное вещество (эфир кислоты);
- натуральный яблочный уксус (имеет низкий кислотный процент, применяется косметологами, кулинарами);
- бальзамический уксус (настоянный на определенных пряных растениях столовый продукт).
Свойства
Прозрачная жидкость обладает резким запахом, имеет плотность 1,05 г/см2. Физические свойства уксусной кислоты обуславливают ее замерзание при температуре 16,6 градусов, при этом субстанция приобретает вид прозрачных кристаллов, напоминающих лед (из-за этого концентрированную кислую жидкость называют ледяной). Кислота имеет способность активно поглощать влагу из воздуха, она может нейтрализовать основные окислы и гидраты, и, кроме того, вытеснять из углекислых солей углекислоту.
Чем опасна уксусная кислота. Когда вреден столовый уксус
 Высокий или низкий уровень кислотности желудка имеет значение. Человеку с кислой средой желудка употреблять уксус не рекомендуется. Это нарушит кислотно-щелочной баланс и спровоцирует развитие язвы. Употребление продукта значительно ухудшает самочувствие людей с такими болезнями:
Высокий или низкий уровень кислотности желудка имеет значение. Человеку с кислой средой желудка употреблять уксус не рекомендуется. Это нарушит кислотно-щелочной баланс и спровоцирует развитие язвы. Употребление продукта значительно ухудшает самочувствие людей с такими болезнями:
- гастрит;
- панкреатит;
- язва желудка и двенадцатиперстной кишки;
- холецистит;
- гастроэнтерит.
При нарушении функций печени также нежелательно употреблять кислоту. А уксусные диеты представляют опасность для здоровья. Если часто кушать блюда с содержанием уксуса, это может нарушить функциональность всего желудочно-кишечного тракта.
Вещество повреждает слизистую оболочку желудка, вызывая изжогу и интенсивную боль. Вред наносит уксусная кислота, если попадает в желудок натощак, когда секреция желудочного сока повышена.
При низком уровне кислотности в желудке небольшое количество продукта можно употреблять в приготовленных блюдах. В этом случае повышение кислотности полезно и не приведет к обострению заболевания.
Абсолютные противопоказания к употреблению уксуса:
- болезни почек;
- детский и пожилой возраст;
- хронические запоры;
- простатит;
- цистит;
- болезни вен.
Симптомы, которые может вызвать кислота при постоянном применении:
- нарушения зрения;
- желтые кожные покровы;
- развитие кариеса.
В минимальных количествах уксус допускается при:
- артрозах;
- артритах;
- остеохондрозе;
- ревматизме;
- сахарном диабете;
- ожирении;
- гипертонии.