Интересные факты о металлах из таблицы менделеева. Металл против монахов
Интересные факты о металлах из таблицы менделеева. Металл против монахов
Антимониум - серебристо-белый металл, среди химиков больше известный как сурьма. Этот металл известен уже много тысяч лет. Например, археологами доказано, что примерно три тысячи лет назад в Вавилоне из сурьмы делали сосуды. Но чаще, конечно, применялся не чистый металл, а его сульфид - «сурьмяный блеск».
В 1604 году появилось первое описание получения сурьмы из соединений. Это описание было в книге довольно известного монаха, а по совместительству алхимика, Василия Валентина.
Василий Валентин верил, что соединения сурьмы могут помочь очистить организм от «вредоносных начал». Он пытался применять сурьму в качестве лекарства. Например, он считал отличным «рвотным средством» вино, которое было выдержано в сурьмяных сосудах. А как вам «вечные пилюли», которые можно было использовать много раз - они просто проходили весь кишечный тракт? Все эти лекарства Василий использовал на монахах, и некоторых из них забирала мучительная смерть. Вот откуда взялось название «антимониум» - противомонашеский металл.

Сегодня есть мнение, что такого человека как Василий Валентин не существовало, ведь его не было в списках монахов ордена, к которому он себя причислял. Вполне возможно, что все его книги - коллективный труд нескольких алхимиков.
И ещё интересный факт про сурьму: в России это название произошло от турецкой косметической процедуры - «чернение бровей». И хотя в качестве краски для бровей сурьму употребляли редко, выражение насурьмить брови» довольно часто можно было услышать в быту.
Интересные факты о драгоценных металлах. 15 фактов о драгоценных металлах
2. Золото — это настолько редкий металл, что за один час в мире находят больше железа, чем за всю историю нашли золота. 3. Платину раньше считали «неправильным серебром» и выкидывали в реки или моря, чтобы не путалась под ногами. Только позже, когда ювелиры из Испании обнаружили, что платина отлично сплавляется с золотом, её стали использовать как ювелирное сырье. 4. «Царская водка» — так называют смесь соляной и азотной кислоты. Этот «коктейль» растворяет золото. 5. Интересно, что самородное серебро встречается значительно реже, чем самородное золото, но общее количество золота на Земле гораздо меньше, чем серебра. Вот такой парадокс. 6. В 1828-ом году в России выпускали платиновые монеты достоинством 3,6 и 12 рублей. На тот момент платина стоила вдвое дешевле серебра. 7. Золото — отличный проводник, поэтому является важнейшим сырьем в электропромышленности. 8. На русском языке — «серебро», на английском — «сильвер», на немецком — «зильбер» — все эти слова происходят от древнеиндийского слова «сарпа», которое обозначало Луну и серп. 9. В Древнем Египте золото считали частичками богов, поэтому владеть им не разрешалось никому, кроме фараона. 10. Самый крупный самородок серебра был найден в Чили и весил 1420 килограмм. 11. Благородные металлы, такие как золото, платина, серебро и палладий не вступают в химическую реакцию с телом. Именно поэтому эти металлы активно используют в медицине и ювелирной промышленности. 12. Олимпийские медали, врученные в 1912 году, были изготовлены из чистого золота. В современном спортивном мире медали покрывают всего лишь 6 граммами этого металла. 13. В 1933 году Франк Рузвельт подписал указ, который запрещал гражданам США хранить у себя золото. Нарушение этого указа каралось штрафом в 10 тысяч долларов или десятью годам лишения свободы. 14. Россия является лидером по добыче и поставке палладия на мировой рынок. 15. Золото 999-ой пробы настолько мягкое, что его с легкостью можно поцарапать ногтем. 1. Благородные металлы — металлы, не подверженные коррозии и окислению, что отличает их от большинства металлов. Все они являются также драгоценными металлами, благодаря их редкости. Основные благородные металлы — золото, серебро, а также платина и остальные 5 металлов платиновой группы — (рутений, родий, палладий, осмий, иридий). Некоторые авторы относят к благородным металлам также и технеций, который не встречается в природе (к тому же он радиоактивен с малым периодом полураспада).
1. Благородные металлы — металлы, не подверженные коррозии и окислению, что отличает их от большинства металлов. Все они являются также драгоценными металлами, благодаря их редкости. Основные благородные металлы — золото, серебро, а также платина и остальные 5 металлов платиновой группы — (рутений, родий, палладий, осмий, иридий). Некоторые авторы относят к благородным металлам также и технеций, который не встречается в природе (к тому же он радиоактивен с малым периодом полураспада).
10 интересных фактов о неметаллах. 10 интересных фактов, о химическом элементе Азоте.

Азот - это очень важный элемент, имеющий особое биологическое значение для всех живых существ, а так же, он играет особую роль в современной промышленности. В периодической системе химических элементов Д.И. Менделеева азот находится во II периоде, V группе, главной подгруппе. Но, что же в нем такого особенного? Возможно десять ниже перечисленных фактов об азоте, помогут пролить свет на это вопрос.
1. В конце XVII века, три независимых друг от друга исследователя смогли получить азот во время своих опытов. Имена этих исследователей: Генри Кавендиш, Джозеф Пристли и Даниэль Резерфорд. В 1772 году Генри Кавендиш провёл следующий опыт: он многократно пропускал воздух над раскалённым углём, затем обрабатывал его щёлочью, в результате получался остаток, который Кавендиш назвал удушливым воздухом. С позиций современной химии ясно, что в реакции с раскалённым углём кислород воздуха связывался в углекислый газ, который затем поглощался щёлочью. При этом остаток газа представлял собой по большей части азот. Таким образом, Кавендиш выделил азот, но не сумел понять, что это новое простое вещество (химический элемент). В результате подобного эксперимента азот был получен и Джозефом Пристли и кстати схожие эксперименты в то время проводил так же Карл Шееле. Однако, лишь Даниэль Резерфорд в том же 1772 г. в своей диссертации «Испорченный воздух» подробнее всех описал свойства полученного им вещества: оно не реагирует со щелочами, не поддерживает горение и непригодно для дыхания. Именно поэтому он и стал считаться первооткрывателем азота. Слово «азот» происходит от греческих терминоэлементов а – отрицающий, зоэ – жизнь. Позже, Лавуазье предложил латинское название данного элемента Nitrogenium. Поэтому в периодической системе азот обозначается символом N. Как простое вещество азот образует двухатомные молекулы N2.

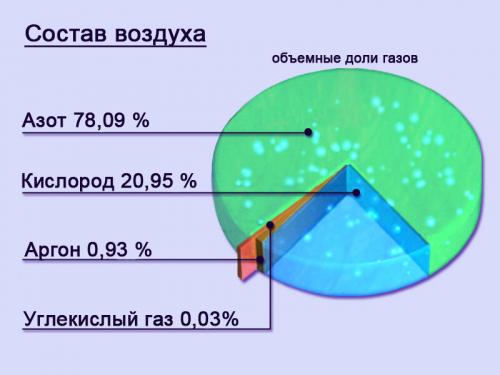
2. По объему азот занимает 4/5 земной атмосферы. Значительные количества азота содержатся в водах мирового океана и в земной коре. 2.5% массы всех живых организмов приходится на азот.
3. Как правило, чистый азот совершенно безвреден для человека. В конце концов, на 78.1% из него состоит воздух, которым мы дышим. В обычном состояние это газ, без цвета, вкуса и запаха. Однако, при высокой концентрации в воздухе, азот может вызывать чувство опьянения, удушья и даже привести к смерти. Так же страшен азот и при кессонной болезни ныряльщиков на глубину.
4. Раньше азот получали из множества различных минеральных веществ. Например, при разложение нитрита аммония:
NH4NO2 = N2 + H2O
При нагревание дихромата калия с сульфатом аммония:
K2Cr2O7 + (NH4)2SO4 = (NH4)2Cr2O7 + K2SO4
(NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O
При пропускание аммиака над оксидом меди (II):
3CuO + 2NH3 = N2 + 3Cu + 3H2O
И т.д.
Однако сейчас примерно миллиард тон азота в год добываются прямо из атмосферы.
5. Мгновенная заморозка чего бы то ни было в жидком азоте, это распространенный кинематографический миф. Жидкий азот действительно имеет очень низкую температуру (-192 градуса Цельсия), но и теплоемкость этого газа низка настолько, что время замораживания даже небольших предметов исчисляется множеством минут.
Активнее всего жидкий азот используется в различных охлаждающих аппаратах, так как инертность азота в отношение других веществ делает его идеальным хладагентом.

6. Азот – очень эффективное средство пожаротушения. Пожары в городе им тушат редко, так как газ сложно оперативно доставить к очагу возгорания и он быстро испаряется на открытой местности. Однако, внутри шахт такой метод тушения пожаров применяется очень часто.
7. Оксид азота (I) (N2O), так же известный как закись азота или веселящий газ, используется для наркоза и улучшает работу двигателей автомобилей. Сам он не горит, но очень хорошо поддерживает горение.
Оксид азота (II) (NO) – очень ядовитое вещество. Однако, в микродозах он содержится во всех живых организмах. В теле человека монооксид азота вырабатывается для нормализации работы сердца, а так же для предотвращения гипертонии и инфарктов.
8. Огромные количества получаемого сегодня азота расходуются на производства садовых удобрений и взрывчатых веществ.
9. А знаете ли вы, что в трубочке ртутного медицинского градусника, помимо серебристого вещества ртути находится так же бесцветный газ азот.

10. Азот, вместе с водородом, кислородом и гелием являются четверкой самых распространенных элементов во Вселенной.
На этом все. Если вам понравилась данная статья, ставьте лайки, пишите в комментариях и не забывайте подписываться на мой канал.